Untuk mengubah energi yang terkandung dalam asam lemak menjadi energi ikatan ATP, terdapat jalur metabolisme oksidasi asam lemak menjadi CO 2 dan air, yang erat kaitannya dengan siklus asam trikarboksilat dan rantai respirasi. Jalan ini disebut β-oksidasi, Karena atom karbon ke-3 dari asam lemak (posisi β) dioksidasi menjadi gugus karboksil, sedangkan gugus asetil, yang meliputi C 1 dan C 2 dari asam lemak asli, dibelah dari asam.
Skema dasar β-oksidasi
Reaksi β-oksidasi terjadi di mitokondria sebagian besar sel tubuh (kecuali sel saraf). Untuk oksidasi, digunakan asam lemak yang masuk ke sitosol dari darah atau muncul selama lipolisis TAG intraselulernya sendiri. Persamaan keseluruhan untuk oksidasi asam palmitat adalah sebagai berikut:
Palmitoyl-SCoA + 7FAD + 7NAD + + 7H 2O + 7HS-KoA → 8Asetil-SCoA + 7FADH 2 + 7NADH
Tahapan oksidasi asam lemak
1. Sebelum menembus matriks mitokondria dan teroksidasi, asam lemak harus mengaktifkan dalam sitosol. Ini dilakukan dengan menempelkan koenzim A ke dalamnya untuk membentuk asil-SCoA. Acyl-SCoA adalah senyawa energi tinggi. Irreversibilitas reaksi dicapai dengan hidrolisis difosfat menjadi dua molekul asam fosfat.
Asil-SCoA sintetase terletak di retikulum endoplasma, di membran luar mitokondria dan di dalamnya. Ada berbagai sintetase khusus untuk asam lemak yang berbeda.
reaksi aktivasi asam lemak
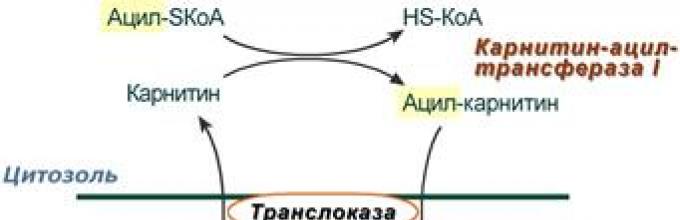
2. Asil-SCoA tidak dapat melewati membran mitokondria, sehingga ada cara untuk mentransfernya dengan kombinasi zat seperti vitamin karnitin. Membran luar mitokondria mengandung enzim karnitin asiltransferase I.

Pengangkutan asam lemak yang bergantung pada karnitin ke dalam mitokondria
Carnitine disintesis di hati dan ginjal dan kemudian diangkut ke organ lain. Di dalam intrauterin periode dan di tahun-tahun awal nilai kehidupan karnitin bagi tubuh sangat tinggi. Pasokan energi sistem saraf milik anak-anak organisme dan, khususnya, otak dilakukan karena dua proses paralel: oksidasi asam lemak yang bergantung karnitin dan oksidasi glukosa aerobik. Karnitin diperlukan untuk pertumbuhan otak dan sumsum tulang belakang, untuk interaksi semua bagian sistem saraf yang bertanggung jawab atas pergerakan dan interaksi otot. Ada penelitian yang menghubungkan kekurangan karnitin lumpuh otak dan fenomena kematian dalam buaian".
Anak kecil, bayi prematur, dan anak dengan berat lahir rendah sangat sensitif terhadap defisiensi karnitin. Cadangan endogen mereka dengan cepat habis dalam berbagai situasi stres (penyakit menular, gangguan pencernaan, gangguan makan). Biosintesis karnitin sangat terbatas karena kecil massa otot dan asupan makanan tidak mampu mempertahankan tingkat darah dan jaringan yang memadai.
3. Setelah berikatan dengan karnitin, asam lemak diangkut melintasi membran oleh translokase. Di sini, di sisi dalam membran, enzim karnitin asiltransferase II kembali membentuk asil-SCoA, yang memasuki jalur β-oksidasi.
4. Proses itu sendiri β-oksidasi terdiri dari 4 reaksi, berulang secara siklis. Mereka berturut-turut oksidasi(asil-SCoA dehidrogenase), hidrasi(enoyl-SCoA-hidratase) dan lagi oksidasi Atom karbon ke-3 (hidroksiasil-SCoA dehidrogenase). Terakhir, reaksi transferase, asetil-SCoA dibelah dari asam lemak. HS-CoA melekat pada asam lemak yang tersisa (dipendekkan dua karbon), dan kembali ke reaksi pertama. Semuanya diulang sampai dua asetil-SCoA terbentuk pada siklus terakhir.

Urutan reaksi β-oksidasi asam lemak
Perhitungan neraca energi β-oksidasi
Sebelumnya, saat menghitung efisiensi oksidasi, koefisien P/O untuk NADH diambil sama dengan 3,0, untuk FADH 2 - 2,0.
Menurut data modern, nilai koefisien P / O untuk NADH sesuai dengan 2,5, untuk FADH 2 - 1,5.
Saat menghitung jumlah ATP yang terbentuk selama β-oksidasi asam lemak, perlu diperhitungkan:
- jumlah asetil-SCoA yang terbentuk ditentukan oleh pembagian biasa jumlah atom karbon dalam asam lemak dengan 2.
- nomor siklus β-oksidasi. Jumlah siklus β-oksidasi mudah ditentukan berdasarkan gagasan asam lemak sebagai rantai unit dua karbon. Jumlah jeda antar unit sesuai dengan jumlah siklus β-oksidasi. Nilai yang sama dapat dihitung dengan menggunakan rumus (n / 2 -1), dimana n adalah jumlah atom karbon dalam asam.
- jumlah ikatan rangkap dalam asam lemak. Pada reaksi pertama β-oksidasi, pembentukan ikatan rangkap terjadi dengan partisipasi FAD. Jika sudah ada ikatan rangkap dalam asam lemak, maka kebutuhan untuk reaksi ini hilang dan FADH 2 tidak terbentuk. Jumlah FADH 2 yang tidak diterima sesuai dengan jumlah ikatan rangkap. Reaksi yang tersisa dari siklus berjalan tanpa perubahan.
- jumlah energi ATP yang dihabiskan untuk aktivasi (selalu sesuai dengan dua ikatan makroergik).
Contoh. Oksidasi asam palmitat
- karena ada 16 atom karbon, maka selama β-oksidasi, 8 molekul asetil-SCoA. Yang terakhir memasuki TCA, selama oksidasi dalam satu putaran siklus, 3 molekul NADH (7,5 ATP), 1 molekul FADH 2 (1,5 ATP) dan 1 molekul GTP terbentuk, yang setara dengan 10 molekul ATP. Jadi, 8 molekul asetil-SCoA akan memberikan pembentukan 8 × 10 = 80 molekul ATP.
- untuk asam palmitat jumlah siklus β-oksidasi adalah 7. Dalam setiap siklus, 1 molekul FADH 2 (1,5 ATP) dan 1 molekul NADH (2,5 ATP) terbentuk. Memasuki rantai pernafasan, secara total mereka akan "memberikan" 4 molekul ATP. Jadi, dalam 7 siklus, 7 × 4 = 28 molekul ATP terbentuk.
- ikatan rangkap dalam asam palmitat TIDAK.
- 1 molekul ATP digunakan untuk mengaktifkan asam lemak, yang, bagaimanapun, dihidrolisis menjadi AMP, yaitu dihabiskan 2 ikatan makroergik atau dua ATP.
Jadi, menyimpulkan, kita dapatkan 80+28-2 =106 Molekul ATP terbentuk selama oksidasi asam palmitat.
Oksidasi biologis asam lemak dapat dibandingkan dengan pembakaran hidrokarbon: dalam kedua kasus, hasil energi bebas tertinggi diamati. Oksidasi-b biologis dari bagian hidrokarbon asam lemak menghasilkan komponen aktif dua-karbon, yang selanjutnya dioksidasi dalam siklus TCA, dan sejumlah besar ekuivalen pereduksi, yang mengarah pada sintesis ATP dalam rantai pernapasan. Sebagian besar sel aerobik mampu mengoksidasi sempurna asam lemak menjadi karbon dioksida dan air.
Sumber asam lemak adalah lipid eksogen atau endogen. Yang terakhir paling sering diwakili oleh triasilgliserida, yang disimpan dalam sel sebagai sumber cadangan energi dan karbon. Selain itu, sel juga menggunakan lipid membran polar, yang pembaharuan metabolismenya terjadi secara konstan. Lipid dipecah oleh enzim spesifik (lipase) menjadi gliserol dan asam lemak bebas.
b-oksidasi asam lemak. Proses utama oksidasi asam lemak ini dilakukan pada eukariota di mitokondria. Pengangkutan asam lemak melintasi membran mitokondria difasilitasi oleh karnitin(g-trimethylamino-b-hydroxybutyrate), yang mengikat molekul asam lemak dengan cara khusus, akibatnya muatan positif (pada atom nitrogen) dan negatif (pada atom oksigen dari gugus karboksil) dekat dan menetralisir satu sama lain.
Setelah diangkut ke matriks mitokondria, asam lemak diaktivasi oleh CoA dalam reaksi yang bergantung pada ATP yang dikatalisis oleh asetat thiokinase (Gbr. 9.1). Kemudian turunan asil-KoA dioksidasi dengan partisipasi asil dehidrogenase. Ada beberapa asil dehidrogenase berbeda di dalam sel yang spesifik untuk turunan CoA dari asam lemak dengan panjang rantai hidrokarbon yang berbeda. Semua enzim ini menggunakan FAD sebagai gugus prostetiknya. FADH 2 yang terbentuk dalam reaksi sebagai bagian dari asil dehidrogenase dioksidasi oleh flavoprotein lain yang mentransfer elektron ke rantai pernapasan sebagai bagian dari membran mitokondria.
Produk oksidasi - enoyl-CoA terhidrasi di bawah aksi enoyl hydratase dengan pembentukan b-hidroksiasil-KoA (Gbr. 9.1). Ada hidratase enoyl-CoA yang spesifik untuk bentuk cis dan trans dari turunan enoyl-CoA dari asam lemak. Pada saat yang sama, trans-enoyl-CoA secara stereospesifik terhidrasi menjadi L-b-hidroksiasil-CoA, dan isomer cis menjadi D-stereoisomer dari -b-hidroksiasil-CoA-ester.
Langkah terakhir dalam reaksi b-oksidasi asam lemak adalah dehidrogenasi L-b-hidroksiasil-KoA (Gbr. 9.1). Atom b-karbon molekul mengalami oksidasi, oleh karena itu seluruh proses disebut b-oksidasi. Reaksi ini dikatalisis oleh b-hidroksiasil-KoA dehidrogenase, yang spesifik hanya untuk bentuk-L dari b-hidroksiasil-KoA. Enzim ini menggunakan NAD sebagai koenzim. Dehidrogenasi isomer-D dari b-hidroksiasilCoA dilakukan setelah tahap tambahan dari isomerisasinya menjadi L-b-hidroksiasil-KoA (enzim b-hidroksiasil-CoA epimerase). Produk dari tahap reaksi ini adalah b-ketoasil-KoA, yang mudah dibelah oleh tiolase menjadi 2 turunan: asil-KoA, yang lebih pendek dari substrat awal yang diaktifkan dengan 2 atom karbon, dan asetil-KoA-dua- komponen karbon yang dibelah dari rantai asam lemak (Gbr. 9.1). Turunan asil-KoA mengalami siklus reaksi oksidasi-b berikutnya, dan asetil-KoA dapat memasuki siklus asam trikarboksilat untuk oksidasi lebih lanjut.
Dengan demikian, setiap siklus b-oksidasi asam lemak disertai dengan pembelahan fragmen dua karbon (asetil-KoA) dan dua pasang atom hidrogen dari substrat, mereduksi 1 molekul NAD + dan satu molekul FAD. Proses berlanjut hingga rantai asam lemak benar-benar terbelah. Jika asam lemak terdiri dari atom karbon dalam jumlah ganjil, maka b-oksidasi diakhiri dengan pembentukan propionil-KoA, yang, dalam beberapa reaksi, berubah menjadi suksinil-KoA dan, dalam bentuk ini, dapat masuk ke TCA siklus.
Sebagian besar asam lemak penyusun sel hewan, tumbuhan, dan mikroorganisme mengandung rantai hidrokarbon tidak bercabang. Pada saat yang sama, lipid dari beberapa mikroorganisme dan lilin tumbuhan mengandung asam lemak yang radikal hidrokarbonnya memiliki titik cabang (biasanya dalam bentuk gugus metil). Jika ada beberapa cabang, dan semuanya jatuh pada posisi genap (pada atom karbon 2, 4, dll.), Maka proses b-oksidasi terjadi sesuai dengan skema biasa dengan pembentukan asetil- dan propionil-KoA. Jika gugus metil terletak pada atom karbon ganjil, proses b-oksidasi diblokir pada tahap hidrasi. Ini harus diperhitungkan dalam produksi deterjen sintetik: untuk memastikan biodegradasinya yang cepat dan lengkap di lingkungan, hanya opsi dengan rantai hidrokarbon lurus yang diizinkan untuk konsumsi massal.
Oksidasi asam lemak tak jenuh. Proses ini dilakukan sesuai dengan semua hukum b-oksidasi. Namun, sebagian besar asam lemak tak jenuh alami memiliki ikatan rangkap di tempat-tempat tersebut dalam rantai hidrokarbon yang secara berturut-turut menghilangkan bagian dua karbon dari ujung karboksil menghasilkan turunan asil-KoA yang ikatan rangkapnya berada di posisi 3-4. Selain itu, ikatan rangkap asam lemak alami memiliki konfigurasi cis. Agar dapat melakukan langkah dehidrogenasi dengan partisipasi b-hidroksiasil-KoA dehidrogenase, yang spesifik untuk bentuk-L dari b-hidroksiasil-KoA, diperlukan langkah isomerisasi enzimatik tambahan, di mana ikatan rangkap pada turunan CoA molekul asam lemak bergerak dari posisi 3-4 ke posisi 2-3 dan konfigurasi ikatan rangkap berubah dari cis menjadi trans. Metabolit ini berfungsi sebagai substrat untuk enoyl hydratase, yang mengubah trans-enoyl-CoA menjadi L-b-hydroxyacyl-CoA.
Dalam kasus di mana transfer dan isomerisasi ikatan rangkap tidak mungkin dilakukan, ikatan tersebut dipulihkan dengan partisipasi NADPH. Degradasi selanjutnya dari asam lemak terjadi melalui mekanisme oksidasi-b yang biasa.
Jalur minor oksidasi asam lemak. b-Oksidasi adalah jalur utama, tetapi bukan satu-satunya, untuk katabolisme asam lemak. Jadi, pada sel tumbuhan ditemukan proses a-oksidasi asam lemak yang mengandung 15-18 atom karbon. Jalur ini melibatkan serangan primer asam lemak oleh peroksidase dengan adanya hidrogen peroksida, dimana karbon karboksilat dibelah menjadi CO2 dan atom karbon-a dioksidasi menjadi gugus aldehida. Kemudian aldehida dioksidasi dengan partisipasi dehidrogenase menjadi asam lemak yang lebih tinggi, dan prosesnya diulangi lagi (Gbr. 9.2). Namun, jalur ini tidak dapat memberikan oksidasi lengkap. Ini hanya digunakan untuk memperpendek rantai asam lemak dan juga sebagai solusi ketika b-oksidasi diblokir karena adanya gugus metil liontin. Proses tersebut tidak memerlukan partisipasi CoA dan tidak disertai dengan pembentukan ATP.
Beberapa asam lemak juga dapat mengalami oksidasi pada atom karbon-w (w-oksidasi). Dalam hal ini, gugus CH 3 - mengalami hidroksilasi di bawah aksi monooksigenase, di mana asam w-hidroksi terbentuk, yang kemudian dioksidasi menjadi asam dikarboksilat. Asam dikarboksilat dapat dipersingkat di kedua ujungnya melalui reaksi b-oksidasi.

Demikian pula, dalam sel mikroorganisme dan beberapa jaringan hewan, terjadi pemecahan hidrokarbon jenuh. Pada tahap pertama, dengan partisipasi oksigen molekuler, molekul dihidroksilasi untuk membentuk alkohol, yang secara berurutan dioksidasi menjadi aldehida dan asam karboksilat, diaktifkan dengan penambahan CoA, dan memasuki jalur b-oksidasi.
terjadi di hati, ginjal, otot rangka dan jantung, di jaringan adiposa. Di jaringan otak, tingkat oksidasi asam lemak sangat rendah; Glukosa merupakan sumber energi utama dalam jaringan otak.
oksidasi molekul asam lemak dalam jaringan tubuh terjadi pada posisi β. Akibatnya, fragmen dua karbon secara berurutan dibelah dari molekul asam lemak dari sisi gugus karboksil.
Asam lemak, yang merupakan bagian dari lemak alami hewan dan tumbuhan, memiliki jumlah atom karbon genap. Asam semacam itu, yang darinya beberapa atom karbon dibelah, akhirnya melewati tahap asam butirat. Setelah β-oksidasi berikutnya, asam butirat menjadi asetoasetat. Yang terakhir kemudian dihidrolisis menjadi dua molekul asam asetat.
Pengiriman asam lemak ke tempat oksidasinya - ke mitokondria - terjadi dengan cara yang kompleks: dengan partisipasi albumin, asam lemak diangkut ke dalam sel; dengan partisipasi protein khusus (protein pengikat asam lemak, FABP) - transportasi di dalam sitosol; dengan partisipasi karnitin - pengangkutan asam lemak dari sitosol ke mitokondria.
Proses oksidasi asam lemak terdiri dari langkah-langkah utama berikut.
Pengaktifanasam lemak. Asam lemak bebas, terlepas dari panjang rantai hidrokarbonnya, bersifat inert secara metabolik dan tidak dapat mengalami transformasi biokimia apa pun, termasuk oksidasi, hingga diaktifkan. Aktivasi asam lemak terjadi pada permukaan luar membran mitokondria dengan partisipasi ATP, koenzim A (HS-KoA), dan ion Mg 2+. Reaksi ini dikatalisis oleh enzim asil-KoA sintetase:
Sebagai hasil reaksi, terbentuk asil-KoA, yang merupakan bentuk aktif dari asam lemak.
Dipercayai bahwa aktivasi asam lemak berlangsung dalam 2 tahap. Pertama, asam lemak bereaksi dengan ATP membentuk asiladenilat, yang merupakan ester dari asam lemak dan AMP. Selanjutnya, gugus sulfhidril dari KoA bekerja pada asiladenilat yang terikat kuat pada enzim untuk membentuk asil-KoA dan AMP.
Mengangkutasam lemakdi dalam mitokondria. Bentuk koenzim asam lemak, seperti halnya asam lemak bebas, tidak memiliki kemampuan untuk menembus ke dalam mitokondria, di mana sebenarnya terjadi oksidasi. Pembawa asam lemak rantai panjang aktif melintasi membran dalam mitokondria adalah karnitin. Gugus asil ditransfer dari atom belerang CoA ke gugus hidroksil karnitin untuk membentuk asilkarnitin, yang berdifusi melintasi membran mitokondria bagian dalam:

Reaksi berlangsung dengan partisipasi enzim sitoplasma spesifik karnitin asiltransferase. Sudah di sisi membran yang menghadap matriks, gugus asil dipindahkan kembali ke CoA, yang menguntungkan secara termodinamika, karena ikatan O-asil dalam karnitin memiliki potensi transfer gugus yang tinggi. Dengan kata lain, setelah lewatnya asilkarnitin melalui membran mitokondria, reaksi sebaliknya terjadi - pemecahan asilkarnitin dengan partisipasi HS-KoA dan asiltransferase karnitin mitokondria:

Intramitokondriaoksidasi asam lemak. Proses oksidasi asam lemak dalam mitokondria sel mencakup beberapa reaksi enzimatik berturut-turut.
Tahap pertama dehidrogenasi. Asil-KoA dalam mitokondria terutama mengalami dehidrogenasi enzimatik, sedangkan asil-KoA kehilangan 2 atom hidrogen pada posisi α- dan β, berubah menjadi ester CoA dari asam tak jenuh. Jadi, reaksi pertama dalam setiap siklus degradasi asil-KoA adalah oksidasinya oleh asil-KoA dehidrogenase, yang mengarah ke pembentukan enoil-KoA dengan ikatan rangkap antara C-2 dan C-3:

Ada beberapa dehidrogenase asil-KoA yang mengandung FAD, yang masing-masing memiliki spesifisitas untuk asil-KoA dengan panjang rantai karbon tertentu.
Panggunghidrasi. Asil-KoA tak jenuh (enoil-KoA), dengan partisipasi enzim enoil-KoA hidratase, menempelkan molekul air. Akibatnya, β-hidroksiasil-KoA (atau 3-hidroksiasil-KoA) terbentuk:

Perhatikan bahwa hidrasi enoyl-CoA bersifat stereospesifik, mirip dengan hidrasi fumarat dan aconitate (lihat hal. 348). Sebagai hasil hidrasi ikatan rangkap trans-Δ 2, hanya L-isomer dari 3-hidroksiasil-KoA yang terbentuk.
Tahap keduadehidrogenasi. β-hidroksiasil-KoA (3-hidroksiasil-KoA) yang dihasilkan kemudian didehidrogenasi. Reaksi ini dikatalisis oleh dehidrogenase yang bergantung pada NAD +:

Tiolasereaksi. Selama reaksi sebelumnya, gugus metilen dioksidasi pada C-3 menjadi gugus okso. Reaksi tiolase adalah pembelahan 3-oksoasil-KoA dengan bantuan gugus tiol dari molekul KoA kedua. Akibatnya, asil-KoA terpotong oleh dua atom karbon dan terbentuk fragmen dua karbon dalam bentuk asetil-KoA. Reaksi ini dikatalisis oleh asetil-KoA asiltransferase (β-ketotiolase):

Asetil-KoA yang dihasilkan mengalami oksidasi dalam siklus asam trikarboksilat, dan asil-KoA, disingkat oleh dua atom karbon, berulang kali melewati seluruh jalur β-oksidasi hingga pembentukan butiril-KoA (senyawa 4-karbon), yang pada gilirannya dioksidasi hingga 2 molekul asetil-KoA
Dalam satu siklus β-oksidasi, 1 molekul asetil-KoA terbentuk, oksidasi yang dalam siklus sitrat menghasilkan sintesis 12 mol ATP. Selain itu, itu terbentuk 1 mol FADH2 dan 1 mol NADH+H, selama oksidasi yang masing-masing disintesis dalam rantai pernapasan 2 dan 3 mol ATP (total 5).
Jadi, selama oksidasi, misalnya asam palmitat (C16), 7 siklus β-oksidasi, sebagai hasilnya 8 mol asetil-KoA, 7 mol FADH 2 dan 7 mol NADH + H terbentuk. Oleh karena itu, hasil ATP adalah 35 molekul sebagai hasil β-oksidasi dan 96 ATP sebagai hasil dari siklus sitrat, yang secara total sesuai dengan 131 molekul ATP.
Oksidasi asam lemak dapat meningkat secara patologis atau berkurang secara patologis.
Meningkatkan laju oksidasi asam lemak, terutama dengan kekurangan karbohidrat, terjadi:
1. Saat mengonsumsi makanan kaya lemak.
2. Saat berpuasa.
3. Dengan diabetes.
Dalam hal ini, dari asetil-KoA, yang terbentuk selama β-oksidasi asam lemak di hati, sejumlah besar badan keton terbentuk. Akumulasi badan keton menyebabkan asidosis dan disebut ketosis.
menolak laju oksidasi asam lemak diamati pada:
1. Kekurangan karnitin. Itu diamati pada bayi baru lahir, lebih sering bayi prematur. Ini disebabkan oleh pelanggaran biosintesis karnitin, atau oleh "kebocoran" di ginjal.
Gejala:
serangan hipoglikemia yang timbul dari penurunan glukoneogenesis akibat pelanggaran oksidasi asam lemak;
Penurunan sintesis badan keton, disertai dengan peningkatan kandungan asam lemak bebas dalam plasma darah;
myasthenia gravis (kelemahan otot);
akumulasi lipid.
Pengobatan: asupan karnitin di dalam.
2. Penurunan aktivitas karnitin palmitoyltransferase.
Di hati, itu menyebabkan hipoglikemia dan penurunan kandungan badan keton dalam plasma darah.
Di otot - pelanggaran proses oksidasi asam lemak, mengakibatkan kelemahan otot dan perkembangan mioglobinuria.
3. Asiduria dikarboksilat.
Gejala utamanya adalah ekskresi asam dikarboksilat C 6 -C 10 dan hipoglikemia berkembang, tidak terkait dengan peningkatan badan keton.
Etiologi: Tidak adanya di mitokondria asetil-KoA dehidrogenase dari asam lemak rantai menengah, yang disingkat menjadi asam dikarboksilat rantai menengah yang dikeluarkan dari tubuh.
Ini terjadi pada manusia setelah makan buah ackee mentah, yang mengandung toksin hipoglisin, yang menonaktifkan asil-KoA dehidrogenase, mengakibatkan penghambatan proses β-oksidasi.
5. Sindrom Zellweger (sindrom serebrohepatorenal).
Ini adalah penyakit keturunan yang langka di mana peroksisom tidak ada di semua jaringan. Pada pasien yang menderita sindrom Zellweger, asam C 26 -C 28 -polyenoic menumpuk di otak, tk. karena tidak adanya peroksisom, mereka tidak mengalami proses oksidasi asam lemak rantai panjang.
6. Penyakit Refsum.
Penyakit saraf langka. Ini terkait dengan kelainan bawaan dari sistem α-oksidasi, yang mengarah pada akumulasi asam fitanat di jaringan, yang menghalangi sistem β-oksidasi.
Penentuan kadar lipid total dalam plasma darah (serum) dengan reaksi warna dengan reagen sulfofosfovanilin
Total lipid - konsep umum yang mencakup asam lemak non-esterifikasi, trigliserida, fosfolipid, kolesterol bebas dan esterifikasi, sphingomyelin.
Prinsip metode ini: produk dekomposisi lipid tak jenuh terbentuk dengan reagen (terdiri dari asam sulfat, asam fosfat dan vanilin) suatu senyawa, yang intensitas warnanya sebanding dengan kandungan lipid total dalam serum darah.
Reagen:
1. Asam sulfat pekat;
2. Campuran fosfovanillin. 4 volume asam fosfat pekat dicampur dengan satu volume larutan vanillin 6 g/l. Campuran disimpan dalam wadah kaca gelap pada suhu kamar.
3. Larutan referensi triolein, 8 g/l.
Kemajuan definisi
Pada 0,02 ml serum darah tambahkan 1,5 ml asam sulfat pekat. Isinya diaduk dan ditempatkan selama 15 menit dalam bak air mendidih. Setelah hidrolisat didinginkan, 0,1 ml diukur (sampel kontrol 0,1 ml asam sulfat pekat), yang dipindahkan ke tabung reaksi lain yang berisi 1,5 ml reagen fosforvanillin. Setelah pencampuran, sampel diinkubasi selama 50 menit di tempat gelap pada suhu kamar. Kepadatan optik sampel (A 1) dan larutan referensi (A 2) diukur pada fotokolorimeter pada panjang gelombang 510-540 nm dalam kuvet dengan ketebalan lapisan 10 mm terhadap larutan kontrol. Perhitungan dilakukan dengan rumus: .
Kandungan normal dalam serum darah : 4 - 8 g/l.
Nilai klinis dan diagnostik. Perubahan kandungan komponen kuantitatif dan kualitatif indikator ini dalam darah diamati pada banyak penyakit dan kondisi patologis yang tidak dibahas dalam panduan ini. Diaplikasikan ke aktivitas otot ada peningkatan indikator ini setelah aktivitas fisik yang berkepanjangan, yang menunjukkan tingkat masuknya metabolisme lipid dalam suplai energi aktivitas otot. Pada saat yang sama, nilai indikator ini biasanya tidak melampaui batas referensi. Lebih informatif adalah penentuan dinamika pergeseran selama aktivitas fisik, komponen dari indikator ini.
BIOSINTESIS LIPID
Biosintesis lipid (lipogenesis) diperlukan untuk membuat bentuk cadangan. Biosintesis lipid dimulai dengan biosintesis asam lemak.
Biosintesis asam lemak
Sistem sintesis asam lemak terletak di fraksi sitoplasma terlarut dari banyak organ dan jaringan, seperti hati, ginjal, kelenjar susu, dan jaringan adiposa.
Biosintesis asam lemak terjadi dengan partisipasi:
1. NADPH∙H + ;
5. asetil-KoA sebagai substrat dan asam palmitat sebagai produk akhir.
Fitur biosintesis asam lemak
Sintesis asam lemak bukanlah pembalikan sederhana dari reaksi β-oksidasi. Fitur yang paling penting adalah sebagai berikut:
1. Sintesis asam lemak terjadi di sitoplasma, berbeda dengan pemecahan yang terjadi di mitokondria.
2. Produk antara sintesis asam lemak berikatan secara kovalen dengan gugus sulfhidril dari protein pembawa asil (ACP).
3. Banyak enzim untuk sintesis asam lemak pada organisme tingkat tinggi dan manusia diatur menjadi kompleks multi-enzim yang disebut sintetase asam lemak.
4. Secara langsung asetil-KoA hanya digunakan sebagai benih.
5. Rantai asam lemak yang tumbuh diperpanjang dengan perlekatan langsung komponen dua karbon yang berasal dari asetil-KoA. Malonyl-CoA berfungsi sebagai donor aktif komponen dua karbon pada tahap perpanjangan. Reaksi pemanjangan dipicu oleh pelepasan CO 2 .
6. Peran zat pereduksi dalam sintesis asam lemak dilakukan oleh NADPH H+ .
7. Sintesis asam lemak adalah proses siklik yang terjadi pada permukaan sintetase asam lemak.
8. Pemanjangan di bawah aksi kompleks sintetase asam lemak berhenti pada tahap pembentukan palmitat (C 16). Pemanjangan lebih lanjut dan pengenalan ikatan rangkap dilakukan oleh sistem enzimatik lainnya.
Langkah-langkah dalam biosintesis asam lemak
Tahap I - pengangkutan asetil-KoA dari mitokondria ke sitoplasma
Asam lemak disintesis di sitoplasma, dan asetil-KoA dibentuk dari piruvat di mitokondria. Membran mitokondria tidak dapat ditembus oleh asetil-KoA; oleh karena itu, pengangkutan asetil-KoA melalui membran disediakan oleh mekanisme khusus. Peran karnitin dalam pengangkutan asetil-KoA tidak besar, karena hanya mengangkut asam lemak rantai panjang. Masalah ini diselesaikan dengan sintesis sitrat.
Sitoplasma mitokondria
Asetil-KoA + oksaloasetat asetil-KoA + oksaloasetat + ADP + Pn
H2O - C - COOH sitrat + ATP + HSKoA
CH 2 - COOH
Beras. 20. Skema pengangkutan asetil-KoA melintasi membran mitokondria
Sitrat dibentuk dalam matriks mitokondria dengan kondensasi asetil-KoA dan oksaloasetat. Kemudian berdifusi ke dalam sitoplasma, di mana ia dibelah oleh sitrat lyase. Jadi, asetil-KoA dan oksaloasetat ditransfer dari mitokondria ke sitoplasma menggunakan satu molekul ATP.
Sumber NADPH H+ untuk biosintesis asam lemak
Oksaloasetat, yang terbentuk sebagai hasil transfer asetil-KoA ke dalam sitoplasma, harus dikembalikan ke mitokondria. Proses ini berhubungan dengan pembentukan NADPH·H + . Reaksi terjadi di sitoplasma dan berlangsung dalam 2 tahap:
1. Oksaloasetat + NADH H + Malat + NAD +
MDH (dekarboksilasi)
2. Malat + NADP + Piruvat + CO 2 + NADPH H +
Piruvat yang dihasilkan dengan mudah berdifusi ke dalam mitokondria, di mana ia dikarboksilasi menjadi oksaloasetat di bawah aksi piruvat karboksilase (dengan pengeluaran energi ATP).
Piruvat + HCO3 - + ATP Oksaloasetat + ADP + F n
Oksidasi lemak normal dalam tubuh berkaitan erat dengan siklus Krebs. Jalur utama pembentukan oksaloasetat adalah karboksilasi PVC. Untuk pembakaran 1,5 g asam lemak, diperlukan 1 g karbohidrat. Oleh karena itu, ada pepatah di kalangan ahli biokimia bahwa "lemak terbakar dalam nyala karbohidrat".
Oksaloasetat, yang disintesis dalam reaksi ini, kemudian berinteraksi dengan asetil-KoA untuk membentuk sitrat, yang teroksidasi dalam TCA.
Jadi, untuk setiap molekul asetil-KoA yang berpindah dari mitokondria ke dalam sitoplasma, satu molekul NADPH H+ terbentuk. Oleh karena itu, selama transisi 8 molekul asetil-KoA yang diperlukan untuk sintesis asam palmitat, 8 molekul NADPH·H+ terbentuk. 6 molekul lain yang diperlukan untuk proses ini dihasilkan di jalur pentosa fosfat.
Tahap II - pembentukan malonyl-CoA.
Ini adalah reaksi pertama dalam biosintesis asam lemak. Dikatalisis oleh enzim asetil-KoA karboksilase. Koenzimnya adalah biotin. Reaksi terdiri dari karboksilasi asetil-KoA, sumber CO2 adalah bikarbonat.
C \u003d O + HCO 3 - + ATP E - biotin CH 2 + ADP + H 3 PO 4
asetil - KoA malonil - KoA
Beras. 21. Karboksilasi asetil-KoA (koenzim asetil-KoA karboksilase adalah biotin)
Malonyl-CoA pada dasarnya adalah asetil-KoA yang diaktifkan. Energi disimpan terlebih dahulu dalam bentuk gugus karboksil dan dilepaskan selama dekarboksilasi secara langsung selama biosintesis asam lemak. Dalam biosintesis asam lemak lebih lanjut, asetil-KoA digunakan sebagai benih, dan sintesisnya sendiri berasal dari malonil-KoA.
Tahap III - biosintesis asam lemak.
Proses oksidasi asam lemak terdiri dari langkah-langkah utama berikut.
aktivasi asam lemak. Asam lemak bebas, terlepas dari panjang rantai hidrokarbonnya, bersifat inert secara metabolik dan tidak dapat mengalami transformasi biokimia apa pun, termasuk oksidasi, hingga diaktifkan. Aktivasi asam lemak terjadi pada permukaan luar membran mitokondria dengan partisipasi ATP, koenzim A (HS-KoA), dan ion Mg 2+. Reaksi ini dikatalisis oleh enzim asil-KoA sintetase:
Sebagai hasil reaksi, terbentuk asil-KoA, yang merupakan bentuk aktif dari asam lemak.
Tahap pertama dehidrogenasi. Asil-KoA dalam mitokondria terutama mengalami dehidrogenasi enzimatik, sedangkan asil-KoA kehilangan 2 atom hidrogen pada posisi α- dan β, berubah menjadi ester CoA dari asam tak jenuh.

tahap hidrasi. Asil-KoA tak jenuh (enoil-KoA), dengan partisipasi enzim enoil-KoA hidratase, menempelkan molekul air. Akibatnya, β-hidroksiasil-KoA (atau 3-hidroksiasil-KoA) terbentuk:

Tahap kedua dehidrogenasi. β-hidroksiasil-KoA (3-hidroksiasil-KoA) yang dihasilkan kemudian didehidrogenasi. Reaksi ini dikatalisis oleh dehidrogenase yang bergantung pada NAD +:

reaksi tiolase. mewakili pembelahan 3-oxoacyl-CoA dengan bantuan gugus tiol dari molekul CoA kedua. Akibatnya, asil-KoA terpotong oleh dua atom karbon dan terbentuk fragmen dua karbon dalam bentuk asetil-KoA. Reaksi ini dikatalisis oleh asetil-KoA asiltransferase (β-ketotiolase):

Asetil-KoA yang dihasilkan mengalami oksidasi dalam siklus asam trikarboksilat, dan asil-KoA, disingkat oleh dua atom karbon, berulang kali melewati seluruh jalur β-oksidasi hingga pembentukan butiril-KoA (senyawa 4-karbon), yang pada gilirannya dioksidasi hingga 2 molekul asetil-KoA.
Keseimbangan energi. Dengan setiap siklus β-oksidasi, satu molekul FADH 2 dan satu molekul NADH terbentuk. Yang terakhir, dalam proses oksidasi dalam rantai pernapasan dan fosforilasi terkait, memberikan: molekul FADH 2 - 2 ATP dan molekul NADH - 3 ATP, mis. secara total, 5 molekul ATP terbentuk dalam satu siklus. Ketika asam palmitat dioksidasi, 5 x 7 \u003d 35 molekul ATP terbentuk. Dalam proses β-oksidasi asam palmitat, 8 molekul asetil-KoA terbentuk, yang masing-masing "terbakar" dalam siklus asam trikarboksilat, menghasilkan 12 molekul ATP, dan 8 molekul asetil-KoA akan menghasilkan 12 x 8 = 96 molekul ATP.
Jadi, secara total, dengan β-oksidasi asam palmitat lengkap, 35 + 96 = 131 molekul ATP terbentuk. Mempertimbangkan satu molekul ATP yang dihabiskan di awal untuk pembentukan bentuk aktif asam palmitat (palmitoyl-CoA), hasil energi total selama oksidasi lengkap satu molekul asam palmitat dalam kondisi tubuh hewan akan menjadi 131 - 1 = 130 molekul ATP.